Pengertian Hidrolisis : Manfaat Jenis Contoh : Hidrolisis adalah reaksi pengikatan gugus hidroksil / OH oleh sebuah senyawa. Gugus OH dapat didapatkan dari senyawa air. Hidrolisis bisa digolongkan menjadi hidrolisis murni, hidrolisis katalis asam, hidrolisis katalis basa, campuran alkali dengan air dan hidrolisis dengan katalis enzim. Sedangkan menurut fase reaksi yang terjadi diklasifikasikan menjadi hidrolisis fase cair dan hidrolisis fase uap.
Pengertian Hidrolisis
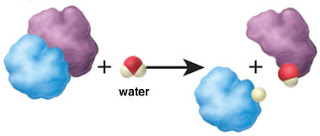
Hidrolisis adalah suatu reaksi kimia dimana H2O (molekul dari air) akan diurai/dipecah kedalam bentuk kation H+ (hidrogen) serta anion OH– (hidroksida) melalui sebuah proses kimiawi. Proses tersebut umumnya dipakai dalam memecah suatu polimer tertentu, khususnya polimer dimana terbuat melalui suatu proses bertahap polimerisasi atau yang dikenal dengan istilah step_growth_polimerization. Istilah hidrolisis sendiri berasal dari kata Yunani yakni hydro yang berarti air serta lysis dengan arti pemisahan.
Secara sederhana arti hidrolisis yaitu proses pembelahan ikatan kimia dengan penambahan air. Sebagai contoh yakni suatu proses sakarifikasi sukrosa. Sakarifikasi adalah suatu pemecahan karbohidrat menjadi komponen molekul gula melalui hidrolisis. Contohnya sukrosa dipecah menjadi fruktosa serta glukosa. Umumnya hidrolisisi maupun sakarifikasi adalah langkah dalam melakukan degradasi zat.
Reaksi kondensasi yaitu suatu reaksi kebalikan hidrolisis yang dimana dua molekul akan bergabung menjadi satu dengan mengeluarkan molekul air saat proses berlangsung. Sehingga suatu perbedaan hidrolisis dan kondensasi yaitu pada kondensasi dua jenis molekul akan menyatu dengan membuang air sedangkan hidrolisis menambahkan air guna memecah molekul yang menyatu.
Biasanya hidrolisis yaitu suatu proses kimia dimana molekul air ditambahkan ke zat. Kadang-kadang penambahan ini mengakibatkan kedua substansi dan molekul air terpecah menjadi dua bagian. Dalam reaksi tersebut, satu fragmen dari molekul target (atau molekul induk) mendapat ion hidrogen.
Manfaat Hidrolisis
Reaksi hidrolisis adalah suatu reaksi kimia yang dipakai untuk menetralkan suatu campuran asam dan basa yang menghasilkan air dan garam. Proses hidrolisis tersebut mempunyai andil yang besar dalam terlaksananya berbagai macam proses penting dan kebutuhan dalam kehidupan sehari-hari.
Berikut ini uraian lebih lanjut terkait beberapa pemanfaatan proses hidrolisis.
- Reaksi hidrolisis antara molekul asam dan basa yang direaksikan dengan air akan membentuk garam dengan rumus kimia NaCl. NaCl ini adalah garam yang dipakai di dapur ibu rumah tangga sebagai pemberi rasa asin dalam makanan.
- Dalam Bidang pertanian reaksi hidrolisis dimanfaatkan dalam suatu penyesuaian pH tanah dengan tanaman yang ditanam. Melalui suatu reaksi hidrolisis akan didapatkan jenis pupuk yang tidak terlalu asam maupun basa. Adapun molekul kimia yang sering dipakai untuk menurunkan pH pupuk yakni pelet padat (NH4)2SO4. Bila garam tersebut direaksikan dalam air, maka ion NH4+ akan terhidrolisis di dalam tanah membentuk NH3 dan H+ yang sifatnya asam.
- Reaksi hidrolisis antara garam yang terbentuk dari HOCl yang adalah asam lemah dengan NaOH yang merupakan basa kuat dengan air akan terjadinya hidrolisis HOCl sehingga akan menghasilkan ion OH- yang sifatnya basa. Sedangkan NaoH sebgai basa kuat tidak terhidrolisis. Garam yang terbentuk melalui penggabungan kedua asam basa terdebut yaitu NaOCl. Garam ini adalah salah satu material yang dimanfaatkan dalam pembuatan bayclin atau sunklin untuk memutihkan pakaian kita.
- Reaksi hidrolisis mempunyai peran penting dalam pemecahan makanan menjadi nutrisi yang mudah diserap. Sebagian besar senyawa organik dalam makanan tidak mudah bereaksi dengan air, sehingga dibutuhkan katalis untuk memungkinkan keberlangsungan proses ini. Katalis organik yang membantu dengan reaksi dalam organisme hidup yang dikenal sebagai enzim. Enzim ini bekerja dengan menerapkan konsep hidrolisis.
- Reaksi hidrolisis ini berperan penting dalam suatu proses pelapukan batuan. Proses ini penting dalam pembentukan tanah, dan membuat mineral penting tersedia bagi tanaman. Berbagai mineral silikat, seperti feldspar, mengalami suatu reaksi hidrolisis lambat dengan air, membentuk tanah liat dan lumpur, bersama dengan senyawa larut.
- Reaksi hidrolisis mempunyai andil dalam penjernihan air. Penjernihan air minum oleh PAM menerapkan prinsip hidrolisis, yakni memakai senyawa aluminium fosfat yang mengalami hidrolisis total.
Jadi, dapat disimpulkan bahwa reaksi hidrolisis terjadi ketika sejumlah senyawa ionik, laksana asam, basa, dan garam dilarutkan dalam molekul air dan dapat menghasilkan sifat yang bervariasi baik tersebut asam, basa, maupun netral. Perbedaan sifat ini menjadi tolok ukur dalam menganalisa peran urgen garam yang terhidrolisis itu dalam kehidupan makhluk hidup.
Jenis Jenis Hidrolisis
Jika ditinjau dari komponen pembentuk garam serta banyak tidaknya garam tersebut bisa diuraikan ketika direaksikan dengan air, maka reaksi hidrolisis bisa dibedakan sebagai berikut ini.
1. Hidrolisis parsial
Hidrolisis parsial yaitu ketika garam direaksikan dengan air hanya salah satu/sebagian ion saja yang mengalami suatu reaksi hidrolisis, sedangkan yang lainnya tidak. Komponen penyusun garam yang mengalami suatu reaksi hidrolisi parsial ini ialah asam lemah dan basa kuat atau sebaliknya.
2. Hidrolisis total
Hidrolisis total adalah suatu reaksi penguraian seluruh garam oleh air, yang mana komponen garam terdiri dari asam lemah dan basa lemah.
Berdasarkan jenis ion-ion yang dihasilkan ketika garam terlarut dalam air, proses hidrolisis bisa dibedakan menjadi beberapa macam berikut ini.
3. Hidrolisis Anion
jika garam yang terdiri dari komponen molekul asam lemah dan basa kuat direaksikan dengan molekul air, maka garam-garam ini hanya akan terhidrolisis sebagian/parsial didalam air dan akan menghasilkan ion yang bersifat basa (OH-). Dengan kata lain, yang terhidrolisis yaitu sedangkan anion dari asam lemah sedangkan kation dari basa kuat tidak terhidrolisis.
Contoh :
CH3COONa(aq) → CH3COO–(aq) + Na+ (aq)
CH3COO– + H2O ↔ CH3COOH + OH–
Na+ + H2O → tidak terjadi reaksi
Dari contoh diatas, menerangkan bahwa CH3COO– yang bertindak sebagai anion asam lemah terhidrolisis membentuk OH– ketika direaksikan dengan molekul air (H2O) sedangakn Na+ yang bertindak sebagai kation dari basa kuat tidak terhidrolisis ketika direkasikan dengan molekul air. Kesimpulannya garam dengan komponen pembentuk asam lemah dan basa kuat, bila direaksikan dengan air akan terhidrolisis sebagian dan menghasilkan ion yang bersifat basa.
4. Hidrolisis Kation
Serupa halnya dengan suatu reaksi hidrolisis antara garam dengan komponen molekul asam lemah dan basa kuat direaksikan dengan molekul air, bila garam dengan komponen penyusun asam kuat dan basa lemah dilarutkan ke dalam molekul air juga akan mengalami suatu hidrolisis parsial dan menghasilkan ion yang sifatnya asam (H+). Hal ini terjadi karena hanya kation dari basa lemah terhidrolisis, sedangkan anion dari asam kuat tidak mengalami suatu hidrolisis.
Contohnya :
NH4Cl → NH4+ + Cl–
NH4+ + H2O ↔ NH4OH + H+
Cl– + H2O → tidak terjadi reaksi
Berdasarkan contoh diatas, bisa disimpulkan bahwa NH4+ yang bertindak sebagai basa lemah terhidrolisis menghasilkan ion yang bersifat asam, yakni H+. Sedangkan Cl- yang sebagai anion asam kuat tidak terhidrolisis.
5. Kation dan Anion Terhidrolisis
Jika garam dengan komponen asam lemah dan basa lemah direaksikan dengan molekul air akan mengalami hidrolisis total. Hal tersebut bisa terjadi dikarenakan kation dari basa lemah maupun anion dari asam lemah bisa terhidrolisis secara sempurna. Reaksi hidrolisis ini menghasilkan ion H+ atau OH-.
Contoh ;
CH3COONH4 → CH3COO– + NH4+
CH3COO– + H2O ↔ CH3COOH + OH–
NH4+ + H2O ↔ NH4OH + H+
Contoh diatas, menerangkan bahwa kedua komponen penyusun garam CH3COO– (anion dari asam lemah) dan NH4+ (kation dari basa lemah) bisa terhidrolsis secara sempurna yang masing-masing berurutan menghasilkan ion yang sifatnya basa (OH–) dan ion yang bersifat asam (H+).
Perlu untuk diketahui, bahwasanya garam dengan komponen asam kuat dan basa kuat yang direaksikan dengan molekul air tidak akan mengalami suatu hidrolisis, dalam arti lain reaksi tersebut sifatnya netral. Peristiwa ini bisa terjadi ketika garam yang mengandung ion logam alkali atau ion logam alkali tanah (kecuali Be2+) dan basa konjugat suatu asamkuat (misalnya, Cl-, Br-, dan NO3-) direaksikan dengan molekul air akan menghasilkan larutan yang bersifat netral.”
Variabel-variabel yang dominan terhadap reaksi hidrolisa :
- Katalisator
Hampir seluruh reaksi hidrolisa membutuhkan katalisator guna mempercepat jalannya reaksi. Katalisator yang digunakan dapat berupa enzim atau asam sebagai katalisator, sebab kerjanya lebih cepat. Asam yang digunakan beraneka aneka mulai dari asam klorida (Agra dkk, 1973; Stout & Rydberg Jr., 1939), Asam sulfat hingga asam nitrat. Yang dominan terhadap kecepatan reaksi ialah konsentrasi ion H, bukan jenis asamnya. Meskipun demikian di dalam industri umumnya digunakan asam klorida. Pemilihan ini didasarkan atas sifat garam yang terbentuk pada penetralan gangguan apa-apa di samping rasa asin andai konsentrasinya tinggi. Karena tersebut konsentrasi harapan dalam air penghidrolisa ditekan sekecil mungkin. Umumnya dipergunkan larutan asam yang mempunyai fokus asam lebih tinggi daripada penciptaan sirup. Hidrolisa pada desakan 1 atm membutuhkan asam yang jauh lebih pekat.
- Suhu dan tekanan
Pengaruh suhu terhadap kecepatan reaksi mengekor persamaan Arhenius.makin tinggi suhu, kian cepat jalannya reaksi. Untuk menjangkau konversi tertentu dibutuhkan waktu selama 3 jam guna menghidrolisa pati ketela rambat pada suhu 100°C. tetapi bila suhunya ditingkatkan sampai suhu 135°C, konversi yang sebesar tersebut dapat dijangkau dalam 40 menit (Agra dkk,1973). Hidrolisis pati gandum dan jagung dengan katalisator asam sulfat membutuhkan suhu 160°C. sebab panas reaksi nyaris mendekati nol dan reaksi berlangsung dalam fase cair maka suhu dan desakan tidak tidak sedikit mempengaruhi keseimbangan.
- Pencampuran (pengadukan)
Supaya zat pereaksi bisa saling bertumbukan dengan sebaik-baiknya, maka butuh adanya pencampuran. Bagi proses batch, urusan ini dapat dijangkau dengan pertolongan pengaduk atau perangkat pengocok (Agra dkk,1973). Apabila prosesnya berupa proses alir (kontinyu), maka pencampuran dilaksanakan dengan teknik mengatur aliran di dalam reaktor agar berbentuk olakan.
- Perbandingan zat pereaksi
Kalau di antara zat pereaksi berlebihan jumlahnya maka ekuilibrium dapat menggeser ke sebelah kanan dengan baik. Oleh karena tersebut suspensi pati yang kadarnya rendah memberi hasil yang lebih baik dikomparasikan kadar patinya tinggi. Bila kadar suspensi diturunkan dari 40% menjadi 20% atau 1%, maka konversi akan meningkat dari 80% menjadi 87 atau 99% (Groggins, 1958). Pada permukaan kadar suspensi pati yang tinggi sampai-sampai molekul-molekul zat pereaksi akan susah bergerak. Bagi menghasilkan pati selama 20%.
Klasifikasi Hidrolisa
Klasifikasi proses hidrolisa dapat dipecah menjadi: (1) Hidrolisa fase gas: Sebagai penghidrolisa ialah air dan reaksi berlangsung pada fase uap. (2) Hidrolisa fase cair: Pada hidrolisa ini, terdapat 4 tipe hidrolisa, yaitu: (a) Hidrolisa murni: Efek dekomposisinya jarang terjadi, tidak seluruh bahan terhidrolisa. Efektif dipakai pada : Reaksi Grigrard dimana air dipakai sebagai penghidrolisa, (b)Hidrolisa bahan-bahan berupa anhidrid asam Laktan dan laktanida. Hidrolisa senyawa alkyl yang memiliki komposisi kompleks, Hidrolisa asam berair.
Pada lazimnya dengan HCl dan H2SO4, dimana tidak sedikit digunakan pada industri bahan pangan, misal: Hidrolisa gluten menjadi monosodium glutamate, Hidrolisa pati menjadi glukosa. Sedangkan H2SO4 tidak sedikit digunakan pada hidrolisa senyawa organik dimana peranan H2SO4 tidak bisa diganti. (c) Hidrolisa dengan alkali berair: Penggunaan fokus alkali yang rendah dalam proses hidrolisa diinginkan ion H+ beraksi sebagai katalisator sementara pada fokus tinggi diinginkan dapat bereaksi dengan asam yang terbentuk. (d) Hidrolisa dengan enzim Senyawa dapat dipakai untuk mengolah suatu bahan menjadi bahan hidrolisa lain. Hidrolisa ini dapat dipakai : Hidrolisa molase, Beer (pati → maltosa/glukosa) dengan enzim amilase.
Aplikasi hidrolisa Pati tidak sedikit digunakan dalam Industri makanan dan minuman memakai sirup glukosa hasil hidrolisis pati sebagai pemanis. Produk akhir hidrolisa pati ialah glukosa yang bisa dijadikan bahan baku untuk buatan fruktosa dan sorbitol. Hasil hidrolisis pati juga tidak sedikit digunakan dalam industri obat-obatan. Dan pun glukosa yang didapatkan dapat dipakai sebagai bahan baku penciptaan bioethanol. Penggunaan asam sebagai penghidrolisa menghasilkan ongkos produksi yang sedikit, tetapi produk yang didapatkan tidak seragam dan tidak sedikit senyawa pati yang bobrok oleh asam tersebut, sedangkan pemakaian enzim sebagai penghidrolisa menghasilkan produk yang seragam, lebih terkontrol, namun ongkos produksi lebih tinggi sebab harga dari enzim sendiri lebih mahal bila dikomparasikan dengan asam.
Hidrolisis Enzim
Enzim ialah biomolekul berupa protein yang bermanfaat sebagai katalis (senyawa yang mempercepat proses reaksi tanpa berakhir bereaksi) dalam sebuah reaksi kimia organik. Molekul mula yang dinamakan substrat bakal dipercepat perubahannya menjadi molekul beda yang dinamakan produk. Jenis produk yang akan didapatkan bergantung pada sebuah kondisi/zat, yang dinamakan promoter. Semua proses biologis sel membutuhkan enzim supaya dapat dilangsungkan dengan lumayan cepat dalam sebuah arah lintasan metabolisme yang ditentukan oleh hormon sebagai promoter.
Enzim bekerja dengan teknik bereaksi dengan molekul substrat guna menghasilkan senyawa intermediat melewati suatu reaksi kimia organik yang memerlukan energi aktivasi lebih rendah, sampai-sampai percepatan reaksi kimia terjadi sebab reaksi kimia dengan energi aktivasi lebih tinggi memerlukan waktu lebih lama.
Sebagai contoh:
X + C → XC (1)
Y + XC → XYC (2)
XYC → CZ (3)
CZ → C + Z (4)
Meskipun senyawa katalis bisa berubah pada reaksi awal, pada reaksi akhir molekul katalis bakal kembali ke format semula.
Sebagian besar enzim bekerja secara khas, yang dengan kata lain setiap jenis enzim melulu dapat bekerja pada satu macam senyawa atau reaksi kimia. Hal ini diakibatkan perbedaan struktur kimia tiap enzim yang mempunyai sifat tetap. Sebagai contoh, enzim α-amilase melulu dapat dipakai pada proses perombakan pati menjadi glukosa.
Kerja enzim diprovokasi oleh sejumlah faktor, terutama ialah substrat, suhu, keasaman, kofaktor dan inhibitor. Tiap enzim membutuhkan suhu dan pH (tingkat keasaman) optimum yang berbeda-beda sebab enzim ialah protein, yang dapat merasakan perubahan format jika suhu dan keasaman berubah. Di luar suhu atau pH yang sesuai, enzim tidak bisa bekerja secara optimal atau strukturnya akan merasakan kerusakan. Hal ini akan mengakibatkan enzim kehilangan kegunaannya sama sekali. Kerja enzim juga diprovokasi oleh molekul lain. Inhibitor ialah molekul yang menurunkan kegiatan enzim, sementara aktivator ialah yang meningkatkan kegiatan enzim. Banyak obat dan racun ialah inihibitor enzim.
Reaksi Hidrolisis terjadi saat suatu asam bertemu dengan basa yang bakal menghasilkan garam dan air yang merubah pH dari gabungan tersebut. Dalam reaksi hidrolisis, terjadi penarikan H+ dan OH- dari senyawa asam dan basa. H+ dan OH- berikatan menjadi air. Sedangkan pembentuk senyawa asam dan basa yang beda bersatu menyusun dari garam gabungan asam basa tersebut. Garam itu dapat mempunyai sifat asam atau basa atau netral tergantung dari sifat – sifat semua campurannya apakan asam kuat, asam lemah, basa kuat, basa lemah.
Contohnya Ketengikan diakibatkan oleh adanya evolusi yang terjadi dari reaksi dengan oksigen di udara-sehingga dinamakan ketengikan oksidatif. Off flavour didapatkan oleh reaksi hidrolisis yang dikatalis oleh enzim-sehingga dinamakan ketengikan hidrolisis. Reaksi hidrolisis dan efek absorpsi bisa dikurangi dengan penyimpanan dingin, transportasi yang baik, pengemasan yang hati-hati dan sterilisasi sedangkan ketengikan oksidatif tidak bisa dikurangi dengan merendahkan temperatur ruang penyimpanan.
Pada reaksi hidrolisis akan didapatkan gliserida dan asam lemak bebas dengan rantai pendek (C4 – C12). Akibat yang dimunculkan dari reaksi ini ialah terjadinya evolusi bau dan rasa dari minyak atau lemak, yaitu munculnya rasa tengik (Djatmiko dan Pandjiwidjaja, 1984). Ketengikan oksidasi yang umum dijumpai yakni reaksi oksidasi pada ikatan rangkap dari asam lemak tidak jenuh. Asam lemak tidak bosan mempunyai ikatan rangkap yang memprovokasi reaksi ini mengakibatkan lemak menjadi keras dan kental.
Peroksida adalah hasil antara yang seringkali dipakai sebagai ukuran tingkat ketengikan (Kaced, et al., 1984). Ketengikan oksidatif adalahreaksi autocatalytic dimana laju reaksi bertambah sejalan dengan bertambahnya waktu penyimpanan. Hal ini diakibatkan karena adanya hasil oksidasi mula yang bisa mempercepat reaksi oksidasi selanjutnya, dan reaksi ini dikenal sebagai reaksi berantai (Schultz, et.al., 1962).
Ketengikan hirdrolisis diakibatkan oleh hidrolisis trigliserida, adanya uap air dan pembebasan asam lemak bebas. Dalam reaksi hidrolisis, lemak dan minyak akan diolah menjadi asam-asam lemak bebas dan gliserol. Reaksi hidrolisis mengakibatkan kehancuran lemak dan minyak. Ini terjadi sebab ada terdapat sebanyak air dalam lemak dan minyak tersebut.
Kerusakan lemak yang utama ialah timbulnya bau dan rasa tengik yang dinamakan proses ketengikan. Hal ini diakibatkan oleh proses otooksidasi radikal asam lemak tidak bosan dalam minyak. Otooksidasi dibuka dengan pembentukan faktor-faktor yang bisa mempercepat reaksi laksana cahaya, panas, peroksida lemak atau hidroperoksida, logam-logam berat, dan enzim- enzim lipoksidase.
Oksidasi dapat dilangsungkan bila terjadi kontak antara sebanyak oksigen dengan lemak atau minyak . terjadinya reaksi oksidasi ini akan menyebabkan bau tengik pada lemak atau minyak. Reaksi oksidasi lemak akan dilangsungkan dalam tiga tahap. Pada etape permulaan terjadi reaksi pembentukan radikal lemak bebas dan pemisahan hidrogen dari lemak yang tidak jenuh.
Fungsi Hidrolisis
Hidrolisis adalah suatu reaksi kimia di mana suatu senyawa dipecah menjadi dua atau lebih bagian melalui interaksi dengan air. Proses ini sering melibatkan pemecahan ikatan kimia dalam senyawa dengan menambahkan molekul air. Hidrolisis dapat terjadi pada berbagai jenis senyawa, termasuk garam, ester, protein, dan karbohidrat. Berikut adalah beberapa fungsi umum dari hidrolisis:
1.Pemecahan Senyawa Organik:
- Ester Hidrolisis: Ester adalah senyawa organik yang dapat mengalami hidrolisis, menghasilkan asam dan alkohol.
- Protein Hidrolisis: Protein dapat dihidrolisis menjadi asam amino melalui reaksi hidrolisis. Proses ini umumnya terjadi dalam pencernaan makanan di dalam tubuh.
2.Metabolisme dan Pencernaan:
- Hidrolisis Glikosida: Dalam pencernaan karbohidrat, hidrolisis glikosida terjadi, memecahkan ikatan antara gula-gula dalam polisakarida, seperti amilum, menjadi monosakarida.
- Hidrolisis Lipida: Lemak dan minyak dapat dihidrolisis menjadi asam lemak dan gliserol, memungkinkan penyerapan nutrisi di saluran pencernaan.
3.Pembersihan Air dan Limbah:
- Hidrolisis Garam: Beberapa garam dapat mengalami hidrolisis, menghasilkan ion hidrogen atau ion hidroksida dan mengubah keasaman atau kebasaan larutan.
- Hidrolisis Amonium: Amonium hidrolisis dapat terjadi dalam pengolahan air limbah, menghasilkan amonia yang dapat dihilangkan dari air.
4.Reaksi Kimia dalam Sel:
- Hidrolisis Adenosin Triphosphate (ATP): ATP, molekul pembawa energi dalam sel, dapat mengalami hidrolisis untuk melepaskan energi yang diperlukan dalam berbagai proses seluler.
- Hidrolisis GTP (Guanosin Triphosphate): Mirip dengan ATP, GTP dapat mengalami hidrolisis untuk menyediakan energi dalam proses biokimia seluler.
5.Industri dan Produksi Kimia:
- Hidrolisis Asam dan Basa: Dalam industri kimia, hidrolisis dapat digunakan untuk menghasilkan produk yang diinginkan dengan memanfaatkan sifat reaktif asam atau basa air.
Hidrolisis memiliki peran penting dalam berbagai proses biologis, industri, dan lingkungan. Melalui reaksi ini, senyawa kompleks dapat dipecah menjadi komponen-komponen yang lebih sederhana, memungkinkan penggunaan atau pengolahan lebih lanjut.


