Berdasarkan tingkat keasamannya, suatu zat dibedakan menjadi 2, yakni zat asam dan zat basa. Zat asam adalah zat yang memiliki ukuran pH kurang dari 7, sementara zat basa adalah zat yang memiliki ukuran pH lebih dari 7. Dalam kehidupan sehari-hari, kita telah akrab dengan zat asam maupun zat basa, misalnya ketika mandi, kita ternyata menggunakan sabun yang mengandung senyawa basa, atau ketika meminum minuman bersoda, ternyata kita meminum larutan asam.
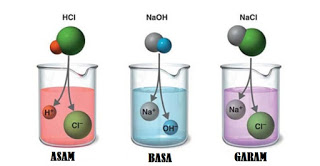
Pengertian Asam
Asam dalam pelajaran kimia adalah senyawa kimia yang bila dilarutkan dalam air akan menghasilkan larutan dengan pH lebih kecil dari 7. Dalam definisi modern, asam adalah suatu zat yang dapat memberi proton (ion H+) kepada zat lain (yang disebut basa), atau dapat menerima pasangan elektron bebas dari suatu basa. Atau Asam adalah zat (senyawa) yang menyebabkan rasa masam pada berbagai materi. Contoh asam : jeruk nipis, lemon, dan tomat.
Ciri – ciri :
- Rasanya asam
- Dapat menimbulkan korosif
- Mengubah kertas lakmus biru menjadi merah
- Ph < 7
- Menghasilkan ion H+
- Jenis larutan asam : – Asam kuat – Asam astrat
Pengertian Basa
Basa adalah senyawa kimia yang menyerap ion hidronium ketika dilarutkan dalam air. Basa memiliki pH lebih besar dari 7. Atau Basa adalah zat (senyawa) yang dapat bereaksi dengan asam, menghasilkan senyawa yang disebut garam. Contoh basa : sabun mandi, sabun cuci, sampo, pasta gigi, pupuk, obat mag.
Ciri – ciri :
- Rasanya pahit
- Terasa licin di kulit
- Mengubah kertas lakmus merah menjadi biru
- Menghasilkan OH- dalam air
Jenis larutan basa : Basa kuat – Basa lemah
Perbedaan Asam dan Basa
1. Perbedaan Rasa Perbedaan asam dan basa yang paling gampang kelihatan terletak pada rasa keduanya. Zat asam, cocok namanya tentulah mempunyai rasa yang masam andai dicicip dengan lidah. Contoh sederhananya ialah vitamin C yang berisi senyawa askorbat, saat Anda menghisap zat ini, Anda tentu akan menikmati rasa asam yang kuat. Sementara zat basa lazimnya mempunyai rasa pahit. Jika tak percaya, letakan secuil saja sabun mandi ke lidah Anda. Rasa pahit yang tak tertahankan tentu akan langsung kita rasakan.
2. Kertas Lakmus Kertas lakmus ialah indikator keasaman yang sangat sering digunakan. Kertas lakmus sendiri terdapat 2 jenis, yakni kertas lakmus merah dan kertas lakmus biru. Senyawa atau zat asam lazimnya akan dapat memerahkan kertas lakmus biru dan tidak merubah warna kertas lakmus merah. Sementara senyawa atau zat basa lazimnya akan dapat membirukan kertas lakmus merah dan tidak merubah warna kertas lakmus biru.
3. Perbedaan Sifat Perbedaan asam dan basa juga dapat kita lihat dari sifatnya. Sifat asam ialah korosif atau bisa mengikis benda beda (terutama logam) yang bersentuhan dengannya. Sementara sifat basa ialah kaustik atau bisa merusak kulit. Kedua sifat asam dan basa ini mesti kita pahami andai tengah sedang di laboratorium. Sifat-sifat itu sangat riskan jika kita tidak menyimak kesehatan dan keselamatan kerja.
4. Reaksi dengan Air Perbedaan asam dan basa pun dapat anda lihat dari hasil reaksi dua-duanya dengan air. Bila senyawa asam dilarutkan ke dalam air, maka bakal terjadi ionisasi yang menghasilkan ion H+, sedangkan bila senyawa basa dilarutkan ke dalam air, maka ion yang terbentuk ialah ion OH-
SIFAT SERTA CIRI – CIRI ASAM DAN BASA
1. Sifat dan ciri-ciri Asam
Sifat dan ciri-ciri asam ialah sebagai berikut:
a. Memiliki rasa yang asam
Sifat yang sangat mencirikan asam ialah terasa asam bila dialami indra pengecap. Contohnya: Cuka adalahsalah satu asam yang tidak jarang kita temukan dalam kehidupan sehari – hari. Dalam ilmu kimia, cuka dikenal dengan nama asam asetat (asam etanoat).
b. Dapat Mengubah Warna Indikator
Di samping rasa asam yang dimilikinya, sifat beda dari asam yakni dapat mengolah warna sejumlah zat alami dan zat buatan. Sifat yang bisa merubah warna zat ini yang dimanfaatkan dalam ilmu kimia untuk menyaksikan suatu senyawa mempunyai sifat asam ataukah mempunyai sifat basa. Dalam ilmu kimia sifat asam disaksikan dari senyawa-senyawa kimia yang diperkirakan mempunyai sifat asam. Sifat asam didentifikasi dengan memakai indikator. Indikator yang sangat sering digunakan ialah kertas lakmus. Jika sebuah senyawa mempunyai sifat asam maka kertas lakmus biru bakal menjadi merah, sementara kertas lakmus merah bakal tetap berwarna merah.
c. Dapat Menghantarkan Arus Listrik
Asam bisa menghantarkan arus listrik. Hal tersebut dikarenakan asam dapat mencungkil ion – ion dalam larutannya. Asam powerful adalahelektrolit yang baik. Semakin kuat sebuah asam, bakal semakin baik pula daya hantar listriknya (mempunyai sifat elektrolit yang baik). Contohnya ialah asam sulfat yang ada pada aki mobil.
d. Asam yang Bereaksi dengan Logam Menghasilkan Gas Hidrogen
Senyawa asam direaksikan atau bereaksi dengan sejumlah jenis logam menghasilkan gas hidrogen. Beberapa misal logam yang andai direaksikan dengan asam bakal menghasil gas hidrogen yaitu: Logam magnesium, besi, tembaga dan seng. Akan namun hasil reaksi dua-duanya bukanlah gas hidrogen saja melainkan pun berisi senyawa garam.
Reaksi :
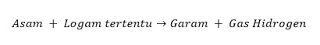
Jika anda mereaksikan dua senyawa asam yang bertolak belakang pada logam yang sama, maka anda akan mendapat hasil yang berbeda. Begitu pun sebaliknya, andai mereaksikan dua logam dengan senyawa asam yang sama. Hal itu diakibatkan perbedaan kekuatan asam yang anda gunakan.
2.Sifat dan Ciri-ciri Basa
Untuk membedakannya dengan asam maka saya dan anda butuh mengetahui sifat dan dan ciri basa. Adapun sifat dan ciri-ciri basa ialah sebagai berikut:
a. Basa miliki rasa yang Pahit
Senyawa basa bilamana dirasakan dengan indra pengecap kita, rasanya bakal pahit. Contohnya saat secara tidak sengaja sabun masuk kedalam mulut. Namun butuh digarisbawahi bahwa dalam meneliti basa tidak disarankan untuk mengerjakan pemeriksaan dengan mencicipinya.
b. Basa terasa licin
Di samping rasanya yang pahit, ternyata basa juga mempunyai sifat licin.
Contohnya : ketika kita memegang sabun, saat disentuh maka sabun itu terasa licin, Basa pembuat sabun ialah natrium hidroksida. Namun dalam praktikum sebenarnya, tidak disarankan mengidentifikasikan senyawa basa dengan menyentuhnya.
c. Bersifat korosif
Untuk mengidentifikasi apakah sebuah senyawa tergolong basa atau tidak, kita paling tidak disarankan untyuk menyentuhnya. Hal ini karena sejumlah senyawa basa adalahjenis senyawa basa yang kuat. Basa powerful ini mempunyai sifat korosif sehingga andai disetuh dapat mengakibatkan iritasi atau terbakar.
d. Basa bisa Mengubah Warna Indikator
Seperti halnya asam, larutan basa pun bakal bereaksi dengan indikator sampai-sampai dapat mengolah warna indikator tersebut. Basa akan mengolah warna kertas lakmus merah menjadi biru, sementara lakmus biru bakal tetap berwarna biru.
e. Menghantarkan Arus Listrik
Di samping senyawa asam ternyata senyawa basa pun adalahpenghantar listrik yang baik, terutama basa kuat. Basa kuat gampang terionisasi dalam air, sampai-sampai dapat mengirimkan arus listrik.
f. Menetralkan Sifat Asam
Senyawa basa dapat dipakai untuk menetralkan asam. Senyawa asam bakal berkurang sifat keasamannya, bahkan dapat pulang menjadi tidak asam andai direaksikan dengan basa. Asam dan basa yang direaksikan bakal menghasilkan garam dan air. Reaksi tersebut disebut dengan reaksi penetralan (netralisasi). Sebagai contohnya ialah kalsium hidroksida direaksikan dengan asam sulfat akan menyusun kalsium sulfat dan air.
Reaksi :

TEORI ASAM DAN BASA
1. Teori Asam Basa Arrhenius
Teori Asam Basa Arrhenius dikemukakan oleh Svante August Arrhenius. Dalam teori tersebut didefinisikan bahwa:
- Asam merupakan senyawa yang jika dilarutkan dalam air melepaskan ion H+.
- Basa merupakan senyawa yang jika dilarutkan dalam air melepaskan ion OH-.
Gas asam klorida (HCl) merupakan salah satu zat yang sangat mudah larut dalam air. HCL atau asam klorida jika dilarutkan dalam air (H2O) akan terurai. HCl dapat terurai menjadi ion H+ dan Cl-.
Oleh karena itu HCl termasuk dalam asam Arrhenius. Akan tetapi berbeda dengan metana (CH4) karena tidak dapat menghasilkan ion H+ dalam air walaupun memiliki atom H, sehingga metana tidak termasuk asam Arrhenius.
Kemudian natrium hidroksida (NaOH) termasuk dalam kategori basa Arrhenius. NaOH merupakan senyawa ionik yang dapat dilarutkan dalam air yang terdisosiasi menjadi ion NA+ dan OH-. Konsep Asam Basa Arrhenius ini hanya pelarutnya terbatas pada air saja.
2. Teori Asam Basa Bronsted-Lowry
Teori asam basa Bronsted Lowry dikemukakan oleh Johannes N. Bronsted dan Thomas M.Lowry pada tahun 1923. Secara terpisah keduanya menyatakan bahwa secara definisi asam basa yang serupa. Konsep yang mereka ajukan harus didasarkan pada fakta bahwa reaksi asam-basa yang melibatkan transfer proton atau ion H+ yang terjadi dari satu zat ke zat lain. Dimana prosesnya melibatkan asam sebagai pendonor dan basa sebagai akseptor (penerima) proton. Sehingga defenisi asam basa Bronsted-Lowry yaitu:
- Asam merupakan donor proton.
- Basa merupakan akseptor proton.
Berikut adalah satu conroh reaksi asam basa menurut Bronsted Lowry :
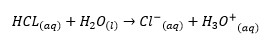
3. Teori Asam Basa Lewis
Teori asam Basa Lewis dikemukakan oleh G. N. Lewis pada tahun 1923. Menurut Lewis definisi asam basa yaitu:
- Asam adalah akseptor yang merupakan pasangan elektron.
- Basa adalah donor yang merupakan pasangan elektron.
Berdasarkan definisi diatas asam berperan sebagai penerima pasangan elektron yang tidak hanya H+. senyawa yang memiliki bilangan orbital 0 pada kulit valensi seperti seperti BF3, juga berperan sebagai asam. Contohnya adalah reaksi antara BF3 dan NH3.
KLASIFIKASI MACAM – MACAM JENIS ASAM DAN BASA
1. Klasifikasi Macam – Macam Jenis Asam
Berdasarkan kekuatannya asam terbagi menjadi dua jenis yaitu:
a. Asam lemah
Contoh asam kuat yaitu: asam sitrat, asam etanoat, asam askorbat dan asam laktat.
b. Asam kuat
Contoh asam lemah yaitu: asam klorida, asam nitrat, asam sulfat dan lain-lain.
2. Klasifikasi Macam – Macam Jenis Basa
Berdasarkan kekuatannya basa terdiri dua jenis yaitu:
a. Basa kuat
Contoh basa kuat yaitu: Litium hidroksida (LiOH), Natrium hidroksida (NaOH), Kalium hidroksida (KOH), Kalsium hidroksida (Ca(OH)2), Stronsium hidroksida (Sr(OH)2) dan Rubidium hidroksida (RbOH), Barium hidroksida (Ba(OH)2) dan Magnesium hidroksida (Mg(OH)2).
b. Basa lemah
Yang dikategorikan dalam basa lemah adalah senyawa basa selain yang telah disebutkan sebagai contoh basa kuat.
Manfaat Senyawa Asam dan Senyawa Basa Dalam Kehidupan Kita Sehari-hari
A.Senyawa Asam
1. Asam Klorida (HCl)
Asam Klorida merupakan asam yang secara alamiah sudah tersedia di dalam lambung kita, asam klorida berguna untuk membunuh kuman atau bakteri yang terdapat di dalam lambung kita.
Asam Klorida juga digunakan sebagai bahan baku pembuatan logam Magnesium ( Mg ).
2. Asam Sulfat (H2SO4)
Digunakan sebagai bahan baku pembuatan pupuk.
Asam Sulfat juga digunakan sebagai elektrolit pada komponen aki.
3. Asam Nitrat (HNO3)
Asam Nitrat digunakan sebagai bahan baku pembuatan senyawa organik seperti nitrobenzena, trinito toulena dan lain-lain.
Asam Nitrat juga digunakan sebagai bahan baku pembuatan bahan peledak seperti TNT.
4. Asam Fosfat (H3PO4)
Asam Fosfat digunakan sebagai bahan baku pembuatan pupuk fosfat .
Asam Fosfat juga digunakan untuk menghilangkan karat pada logam besi.
5. Asam Perklorat (HClO4)
Asam Perklorat digunakan sebagai bahan baku pembuatan bahan bakar roket yaitu ammonium perklorat (NH4ClO4).
6. Asam Asetat (CH3COOH)
Asam Asetat digunakan sebagai bahan penyedap makanan
Asam Asetat juga digunakan untuk memproduksi senyawa ester.
7. Asam Hipoklorit (HClO)
Asam Hipoklorit digunakan sebagai disinfektan dan pemutih pakaian.
8. Asam Benzoat (C6H5COOH)
Asam Benzoat dapat digunakan sebagai disinfektan.
Asam Benzoat juga dapat digunakan sebagai bahan baku pembuatan phenol.
9. Asam Flourida (HF)
Asam Flourida digunakan untuk menghilangkan karat pada logam.
Asam Flourida juga dapat digunakan untuk melarutkan benda-benda yang terbuat dari kaca/silika.
10. Asam Format (HCOOH)
Asam Format digunakan dalam industri tekstil
Asam Format juga digunakan untuk mensintesis
B.Senyawa Basa
1. Natrium Hidroksida (NaOH)
Natrium Hidroksida digunakan sebagai pembersih pada saluran-saluran pipa yang tersumbat oleh lemak/kotoran ( Anti Mampet )
Natrium Hidroksida juga digunakan sebagai bahan baku pembuatan sabun cuci.
2. Kalium Hidroksida (KOH)
Kalium Hidroksida dapat digunakan sebagai bahan baku pembuatan sabun cuci dan sabun mandi.
Biasa digunakan sebagai elektrolit pada baterai alkali.
3. Magnesium Hidroksida (Mg(OH2))
Dapat digunakan sebagai antasid ( obat maag ).
4. Tembaga(II)Hidroksida ( Cu(OH2) )
Digunakan sebagai pigmen biru.
Dapat juga digunakan sebagai fungisida.
5. Kalsium Hidroksida ( Ca(OH)2 )
Digunakan dalam proses water treatment.
6. Barium Hidroksida ( Ba(OH)2 )
Dalam skala labor banyak digunakan untuk membuat senyawa barium lain dan juga sering digunakan untuk titrasi asam lemah.
7. Strontium Hidroksida ( Sr(OH)2 )
Digunakan sebagai stabilisasi dalam industri plastik.
8. Ammonium Hidroksida ( NH3 )
Digunakan sebagai bahan baku pembuatan pupuk.
Digunakan juga sebagai bahan baku pembuatan asam nitrat.
9. Lithium Hidroksida ( LiOH )
Digunakan sebagai elektrolit pada baterai alkali litium.
Juga digunakan sebagai campuran semen.
10. Besi(II)Hidroksida ( Fe(OH)2 )
Digunakan untuk mengendapkan ion beracun selenat dan selenit.


